Troubles Plantaires
La fasciite plantaire / L’aponévrosite plantaire Quelle soit à droite ou à gauche posez sur les 5 zones suivantes : N° 01 1 patch sur
Trois conditions sont nécessaires à la bonne cicatrisation :
Elle va cicatriser spontanément après nettoyage et parage : c’est la cicatrisation dite dirigée. On observe dans l’ordre d’apparition :
La vitesse de croissance de l’épithélium varie de 2 à 10 mm par 24 h en fonction de l’éloignement des berges. Plus elles sont proches, plus la vitesse augmente.
Elle est variable aussi avec la nature et la qualité de la peau (peau du dos plus longue à cicatriser que les paupières par exemple).
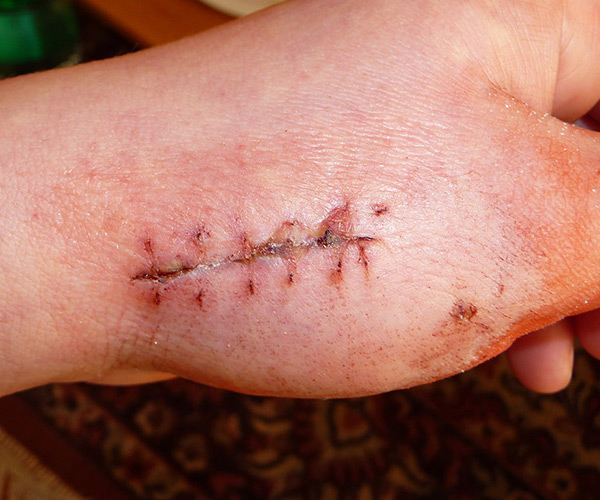
Le processus de cicatrisation débute dès l’agression qui a détruit le revêtement cutané. Différentes phases se succèdent sous la dépendance de facteurs de plus en plus connus, mais malgré tout le mécanisme reste complexe.
Nous allons le schématiser ainsi :
Il est indispensable et doit être respecté. Les variations de la flore au cours de l’évolution détermine le bactériocycle.
En dehors de toute thérapeutique antiseptique ce cycle passe par 3 phases :
– Une première période à cocci GRAM (+) : staphylocoques et streptocoques.
– Une seconde période à bacilles GRAM (-) : notamment le pyocyanique dont la présence est considérée comme favorable s’il reste sur la plaie.
– Une troisiéme période à cocci GRAM (+) exclusivement qui survient à la phase terminale d’épidermisation.
Ainsi, toute plaie utilise des batéries « saprophytes » ou nécessaires à la cicatrisation.
A ne pas confondre avec la surinfection où la flore devient pathogène et virulente.
La rupture cellulaire liée à l’agression des différents tissus, fait apparaître les agents de la protéolyse qui disloquent la substance fondamentale (protéines).
– L’Histamine entraine l’augmentation de la perméabilité capillaire
– La Leucotaxine entraine une vasodilatation brutale
– La Pyrexine entraine la destruction des protéines donnant des poussées thermiques (Calor)
– Les Cytokines (les interleukines) et les facteurs de croissances tissulaires agissent sur la multiplication cellulaire.
– polynucléaires neutrophiles ou microphages : Ils phagocytent, les bactéries et les particules étrangères
– polynucléaires éosinophiles, lymphocytes et plasmocytes : Ils ont une capacité phagocytaire plus faible
– histiocytes ou macrophages : Ils phagocytent les grosses particules
Elles réalisent un halo œdémateux autour des capillaires. Un flux liquidien s’organise de la profondeur vers la surface permettant l’élimination des éléments nécrosés. Ce flux riche en fibrine coagule à la surface et forme l’enduit fibrino-leucocytaire.
C’est un nouveau tissu comblant la perte de substance initiale. 3 zones se forment de la superficie à la profondeur :
A ce stade l’action des substances précédemment décrites s’épuise, d’autres prennent le relais notamment le facteur de croissance épithélial (EGF).
* L’Organisation du bourgeon charnu va finir par involuer, laissant place au derme reconstitué.
Les fibres de collagènes se multiplient et sont entourées de substance fondamentale plus dense. Les vaisseaux s’oblitèrent. Parfois un derme pathologique ou non fonctionnel apparaît.
* Action du myofibroblaste : contraction des berges sous l’influence des facteurs inflammatoires. Les fibroblastes acquièrent alors des propriétés proches de celles de cellules musculaires lisses et deviennent des myofibroblastes qui tendent à rapprocher les berges.
* Régénération de l’épiderme : démarre de la périphérie de la plaie où les cellules basales deviennent actives.
L’épiderme est d’abord formé d’une couche monocellulaire fragile qui inhibe la croissance du bourgeon charnu. Progressivement, plusieurs assises cellulaires se constituent pour aboutir à un épiderme stable.
* La cicatrice : c’est le stade ultime, arrêt du processus au moment où l’équilibre épidermo-conjonctif est rétabli.
Ils sont actuellement de mieux en mieux connus et répertoriés.
Certains sont libérés précocement avec les facteurs de l’inflammation (PDGF : facteur de croissance dérivant des plaquettes, FGF : fibroblast growth factor).
D’autres sont libérés plus tardivement, au niveau du foie notamment (TGF : transforming growth factor, EGF : epidermal growth factor).
Ils sont actuellement de mieux en mieux connus et répertoriés.
Certains sont libérés précocement avec les facteurs de l’inflammation (PDGF : facteur de croissance dérivant des plaquettes, FGF : fibroblast growth factor).
D’autres sont libérés plus tardivement, au niveau du foie notamment (TGF : transforming growth factor, EGF : epidermal growth factor).
Les biopsies cicatricielles montrent que la cicatrice passe par 4 stades :
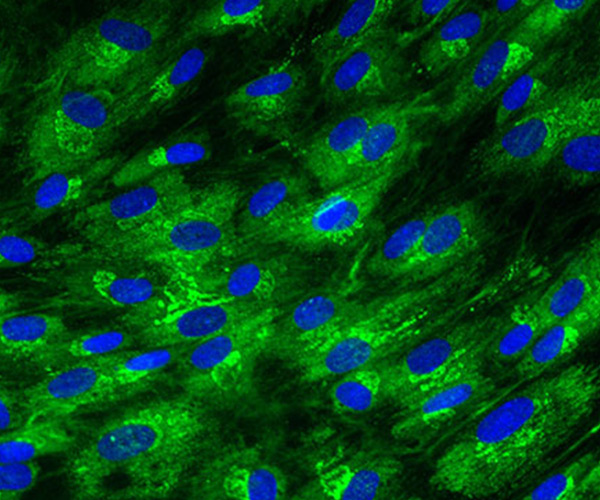
Elle est le siège d’une inflammation chronique et d’une activité prolongée au-delà des délais «normaux».
Initialement la cicatrice se comporte normalement. Poussée inflammatoire vers le 21ème jour mais le processus congestif continue d’augmenter au-delà du 2ème mois. La cicatrice est alors rouge violacée et douloureuse.
L’hypertrophie va s’atténuer à partir du 6ème mois et finir son évolution vers la 2ème année.
Il s’agit donc d’une cicatrice dont la phase inflammatoire est trop intense et trop prolongée mais qui finit par se stabiliser en une cicatrice tolérable, souvent un peu large et épaisse.
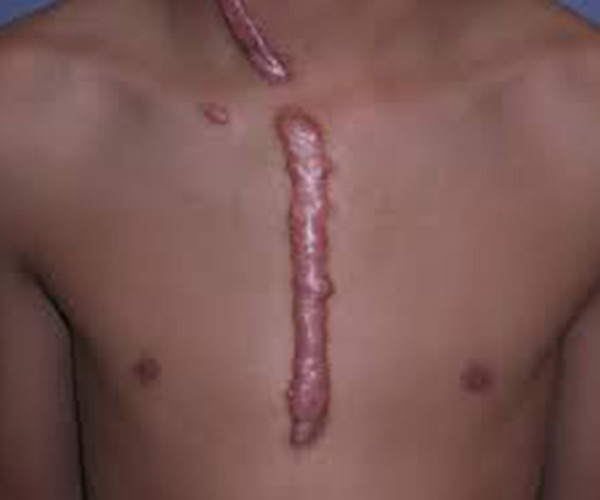
Sachant, qu’après l’âge de 2 ans, la cicatrice va passer presque inévitablement par un stade hypertrophique, il semble intéressant d’essayer de la maîtriser. Tous les moyens qui suivent agissent en diminuant la composante vasculaire de l’inflammation.
– La pressothérapie ou compression cicatricielle.
Application constante d’une pression proche de la pression capillaire. Méthode contraignante mais a l’avantage de son innocuité. En pratique on utilise :
La compression est portée 24 h/24 sauf pour la toilette et dès la cicatrisation terminée avant que ne débute l’hypertrophie. Elle reste cependant efficace lorsque le processus hypertrophique est en cours.
– La kinésithérapie.
Son action est mécanique, sous forme de pétrissage, de malaxage et d’effleurements, elle permet de mobiliser le tissu fibreux. Des pommades peuvent être utilisées (hydratantes, «cicatrisantes») : elles facilitent l’action des doigts et rendent les manipulations moins douloureuses mais ont peu d’effet par elles-mêmes.
– La cure thermale.
Les douches filiformes à forte pression ont une action mécanique. L’action propre des eaux n’est pas unanimement reconnue.
– La corticothérapie.
Elle a certes un effet anti-inflammatoire puissant mais aussi des effets secondaires et reste à manier avec prudence. Son action en surface est immédiate calmant la douleur et le prurit.
– La chirurgie n’est d’aucun secours
C’est une véritable «tumeur» fibreuse cicatricielle qui a tendance à récidiver
C’est une véritable «tumeur» fibreuse cicatricielle qui a tendance à récidiver
La chéloïde tient du fibrome et de l’angiome. Il n’y a pas de maturation des fibroblastes et du collagène et donc on obtient une surproduction
Rien ne peut laisser prévoir l’apparition d’une chéloïde.
Certains facteurs seraient prédisposant.
prototype cutané roux > blond > brun
Imprévisible, la chéloïde a une tendance désespérante à la récidive. Sa dégénérescence sous forme de carcinome épidermoïde plusieurs années après est classique mais rare. Il suffit à justifier sa prévention, notamment chaque fois qu’un facteur favorisant est retrouvé.
– Compression et massages.
Entrepris avant la 3 ème semaine ils ont un rôle préventif comme dans l’hypertrophie. Ils peuvent également freiner la prolifération.
– Ultrasons. Agissant sur le prurit et la douleur. N’ont pas de rôle préventif.
– Les corticoïdes. Ils ont une action certaine et sont actuellement la base du traitement médical mais doivent être utilisés avec précaution en pédiatrie
– La chirurgie.
Le risque de récidive est important et le patient doit en être prévenu.
– Les radiations ionisantes
Elles ont été proposées sous forme de radiothérapie lourde de conséquence et de toute façon contre indiquée dans cette indication chez l’enfant.
Large et déprimée, elle résulte souvent d’un défaut de soutien sous-cutané, d’une hypo vascularisation ou de l’emploi de corticoïdes. Le traitement en est l’excision-suture avec assistance cutanée (stéri-strips ou autre moyen).
L’hyper pigmentation résulte de troubles vasculaires (insuffisance veineuse, difficultés de prise de greffe) ou d’une exposition solaire.
Le prurit peut être considéré comme physiologique en début d’évolution. Il devient parfois invalidant. Les antihistaminiques peuvent être tentés mais pas toujours efficaces. Il faut parfois avoir recours aux neuroleptiques. Les douleurs au froid sont classiques. Il faut éviter l’exposition ou protéger chaudement…Les douleurs nécromateuses nécessitent des reprises chirurgicales.
La cicatrisation et la cicatrice qui en résulte sont des phénomènes complexes dont la physiologie peut être perturbée par différents facteurs qu’il convient de connaître. La cicatrice est la marque visible et indélébile d’un acte chirurgical ou d’un traumatisme. L’enfant va grandir avec et la supporter toute une vie, autant qu’elle soit discrète et bien placée.
Quel que soit l’âge et le type de cicatrice, la Programmation Neuro Fonctionnelle a trouvé la solution pour réhabiliter vos cicatrices, notamment les plus vieilles face auxquelles, il y a longtemps qu’on a baissé les bras.
En effet, nous nous sommes rendu-compte que les cicatrices, au-delà de leur aspect qui peut être fortement inesthétique (chéloïde, hypertrophique, pigmentaire), gardent quasiment toutes, une mémoire traumatique. En effet, même vieilles de plusieurs années, elles peuvent conserver la mémoire du traumatisme initiale et continuer à perturber les fonctions locomotrices (si elles sont sur les membres inférieurs et le ventre), la verticalisation (dos, ventre, torse), les mouvements des bras et mains (quand elles sont situées sur les membres supérieurs).
Afin de savoir si la cicatrice est encore « active » et continue à brouiller un geste ou un mouvement, nous avons mis en place un test de force : le Finger Resist. Il suffit de faire serrer les doigts au patient contre résistance. On observe d’abord sa force développée, puis on touche ou en caresse la cicatrice, sans appuyer et sans générer de douleur. On réalise à nouveau le test de résistance des doigts et on va noter systématiquement une chute de puissance par rapport au test initial.
On peut également demander des mouvements spécifiques, comme se mettre sur une jambe et fléchir le genou, des torsions de bassin, des mouvements de bras. On note l’amplitude et la facilité pour le patient à faire le mouvement choisi. Puis on touche la cicatrice à tester et on observe les déséquilibres, ou les limitations de mouvements induits par l’activation de la cicatrice.
Concrètement, la zone cicatricielle agit en continuant d’envoyer au cerveau des informations de stress comme si l’événement traumatique (parfois vieux de 10 ans) était toujours présent.
Ainsi, bien plus que le seul aspect esthétique, une cicatrice peut continuer à perturber l’organisme par des mouvements incomplets ou parasites, entrainant peu à peu des dysfonctions pathologiques où personne ne soupçonne une cicatrice vieille de 5 à 10 ans qui semble intégrée.
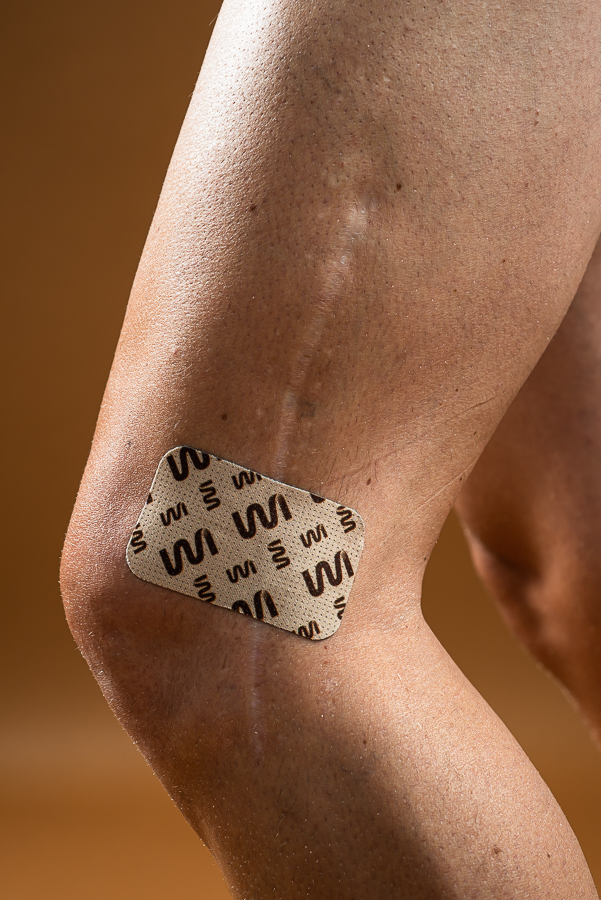
Une fois la cicatrice « active » repérée, il suffit de coller un patch infrarouge Stimcare sur toute sa longueur ou surface. Dès la première minute on note une régularisation de la force musculaire et une libération des mouvements perturbés par la cicatrice, celle-ci étant désactivée par l’action du patch. Ce dernier en renvoyant les infrarouges endogènes, stimule l’eNOsythase qui va entrainer une dilatation des micro capillaires et une réactivation des terminaisons nerveuses. Cela redonne au cerveau une information normale et automatiquement les schémas corporaux naturels sont retrouvés.
Cerise sur le gâteau, si la cicatrice est boursouflée, chéloïde, rouge ou adhérente, l’activation de la microcirculation grâce au renvoie des infrarouges, va peu à peu réactiver l’ensemble des phases de la cicatrisation. Après 2 à 4 mois de port quotidien du patch, on observe une atténuation de la coloration, des épaisseurs, une libération des adhérences, en bref un retour à un cicatrice saine, souple, blanche, normale.
La fasciite plantaire / L’aponévrosite plantaire Quelle soit à droite ou à gauche posez sur les 5 zones suivantes : N° 01 1 patch sur
Contracture / Déchirure/ oedème N° 01 Recouvrez complétement avec 1 à 3 patchs sur la zone gonflée, déchirée ou oedémateuse +1 patch au tiers inférieur du
Tortel Formation
2761 Les Rouvières
26220 Dieulefit France
(hors DOM-TOM)
 par Altazir Ops
par Altazir Ops